Abstract: The article discusses the classification, causes and manifestations of hepatic encephalopathy. The main theories of the pathogenesis of hepatic encephalopathy in the framework of fulminant hepatic insufficiency and hepatic encephalopathy in chronic liver diseases are considered.
Keywords: hepatic insufficiency, hepatic encephalopathy, fulminant (lightning) hepatic insufficiency, cirrhosis of the liver, hyperammonemia, blood-brain barrier, cerebral edema.
Печеночная недостаточность анимает одно из ведущих мест в мире после сердечно-сосудистых и онкологических патологий. Это связано с ухудшением экологического состояния окружающей среды, изменением уровня жизни людей, ухудшением качества продуктов питания, увеличением потребления некачественного алкоголя, широким распространением вирусных инфекций [1, 2].
Широкий спектр нарушений функции печени варьируется от умеренных до молниеносных. Отличительной особенностью течения заболеваний печени является высокая смертность в остром периоде заболевания (90%), а также высокая частота хронизации процесса (цирроз печени или гепатоцеллюлярная карцинома) с развитием инвалидности, ухудшением качества жизни, снижением о его продолжительности [1, 2].
Печёночная энцефалопатия — это нервно-психическое расстройство с нарушением интеллекта, сознания, рефлекторной деятельности и функций жизненно важных органов. Выделяют острую и хроническую печёночную энцефалопатию [1-5].
Разграничивают 4 стадии печеночной энцефалопатии [1-4]:
- Стадия I – продромальная
— начальные изменения в психике характеризуются: замедлением мышления, нарушением поведения, дезориентацией пациента в окружающей действительности, нарушением сна (сонливость днём, бессонница ночью), плаксивость, слабость ума. А, также периодами ступора с неподвижным взглядом. Отличительным и довольно ранним симптомом является изменение почерка (дисграфия). На ЭЭГ, как правило, изменения не определяются.
- Стадия II — начинающаяся кома
— симптомы продромальной стадии усиливаются: возникают судороги и психомоторное возбуждение. Появляются стереотипные движения, например, хлопающий тремор рук (астериксис), ступор. А, так же неопрятность, фамильярность. Может наблюдаться лихорадка и печёночный запах изо рта. ЭЭГ показывает незначительные начальные изменения.
- Стадия III — ступор
— длительный сон, прерываемый редкими пробуждениями. Отмечаются ригидность мышц, похожее на маску лицо. Характерно замедление произвольных движений, грубые нарушения речи (дизартрия), гиперрефлексия и др. На ЭЭГ обнаруживаются глубокие нарушения, форма кривой приближается к изолинии.
- Стадия IV – кома
— развивается потеря сознания и отсутствие реакции на болевой раздражитель, выражены патологические рефлексы. Далее расширение зрачков, угасание рефлексов, снижение артериального давления, возникают патологические типы дыхания Куссмауля или Чейна-Стокса, что может привести к летальному исходу.
В соответствии с этиотропными факторами, приводящими к развитию печёночной энцефалопатии, выделяют следующие типы печеночной недостаточности [5]:
-Тип А
возникает при острой печёночной недостаточности
-Тип В
обусловлен портосистемным шунтированием в отсутствие хронической печёночной недостаточности
-Тип С
наиболее распространённый, обусловленный циррозом печени.
Печеночную энцефалопатию классифицируют [1, 2]:
- «Эпизодическая печёночная энцефалопатия»
интермиттирующие нейропсихические нарушения.
- «Фульминантная (молниеносная) печёночная недостаточность»
быстро нарастающие клинические проявления в условиях фульминантной печёночной недостаточности (как правило, при воздействии гепатотоксичных факторов).
- «Спонтанная печёночная недостаточность»
отсутствие гепатотоксичного фактора и проявления печёночной энцефалопатии.
- «Персистирующую печёночная энцефалопатия»
- длительное сохранение когнитивных нарушений, ограничивающих повседневную активность.
- «Печёночная энцефалопатию, поддающаяся лечению»
- симптомы регрессируют при соответствующей терапии.
- «Минимальная печёночная энцефалопатия»
явные психоневрологические отклонения отсутствуют, однако их выявляют с помощью специальных методов (нейрометрические тесты, электроэнцефалография, вызванные потенциалы и др.). На основании данных, полученных с помощью специальных методов, можно сделать вывод, что распространённость минимальной печёночной энцефалопатии среди пациентов с циррозом печени составляет от 30 до 84%.
Выделяют следующие этиотропные факторы приводящие к возникновению печёночной энцефалопатии [1-3]:
— Первая группа это:
острые вирусные гепатиты В и С, реже гепатит Д, иногда гепатит А и Е, крайне редко другие инфекционные гепатиты (жёлтая лихорадка, лептоспироз, мононуклеоз и др.).
— Ко второй группе относят:
медикаментозные гепатиты (на фоне парацетамола, особенно в комбинации с алкоголем, изониазид, галотан, альдомет и др.).
— третья группа:
алкоголь — реже без предшествующей болезни печени, чаще на фоне хронического алкогольного поражения печени.
— Четвертая группа
Болезнь Вильсона-Коновалова — наследственное заболевание, связанное с нарушением обмена меди в организме, характеризующееся её чрезмерным накоплением в печени, мозге, почках и отравляющим действием на многие внутренние органы (чаще в процесс вовлекается печень и нервная система).
— пятая группа:
Синдром Бадда-Киари — обструкция (тромбоз) печёночных вен, которая наблюдается на уровне их впадения в нижнюю полую вену и приводит к нарушению оттока крови из печени.
— Шестая группа:
Жировая дистрофия печени беременных.
Согласно современным представлениям, механизмом печеночной энцефалопатии при хронических заболеваниях печени является повреждающее действие аммиака на астроциты. Известно, что только около 7% образующегося в организме аммиака проходит через мозговую ткань, не вызывая нарушений в ее структурных и функциональных взаимодействиях. Повреждение печени и развитие шунтирования приводят к тому, что кровь, содержащая большое количество аммиака, попадает в системный кровоток. Гипераммониемия, развивающаяся у пациентов с циррозом и портосистемным шунтированием, связана с повышенной абсорбцией аммиака в кишечнике, нарушением детоксикации аммиака в печени (снижение активности ферментов цикла синтеза мочевины) (рис. 1) и снижением степени связывания аммиака в гипотрофических скелетных мышцах (снижение активности глутаминсинтетазы) [1-3, 5].
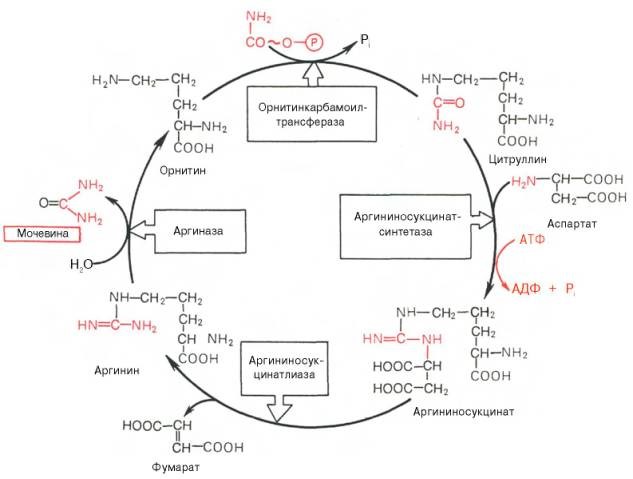
Рисунок 1. Синтез мочевины в норме (Т.Т. Березов, Б.Ф. Коровкин, 2011г.)
Образование аммиака в мышечной ткани имеет ключевое значение при циррозе печени. Гипераммониемия играет важную роль в патогенезе печеночной энцефалопатии, способствует развитию комы при желудочно-кишечном кровотечении или употреблении чрезмерного количества белка при циррозе печени. Гипераммониемия способствует увеличению содержания аммиака в головном мозге, обусловленному нарушением проницаемости гематоэнцефалического барьера, и его токсическому действию на астроциты [5]. При печеночной энцефалопатии в веществе головного мозга и спинномозговой жидкости увеличивается содержание метаболитов аммиака, особенно глутамина и α-кетоглутарата. Астроциты (самые многочисленные клетки в головном мозге) выполняют такие важные функции, как поддержание целостности гематоэнцефалического барьера, дезактивация аммиака, выработка нейромедиаторов и обеспечение связей между нейронами. При гипераммониемии в астроцитах происходят морфологические и функциональные изменения, в частности в ядре [1-3].
Предполагается, что тяжесть нервно-психических расстройств при печеночной недостаточности коррелирует со степенью гипераммониемии и выраженностью изменений в астроцитах. Тем самым подтверждая, что синдром печеночной энцефалопатии является прямым следствием дисфункции астроцитов. В астроцитах глутамат превращается в глутамин при участии глутаминсинтетазы. Гипераммониемия повышает активность глутаминсинтетазы и изменяет активность других ферментов, а именно белка-носителя глутамата. В результате повышается уровень глутамата во внеклеточном пространстве. Исследования с использованием МР-спектроскопии позволяют зафиксировать внеклеточное происхождение отека головного мозга и его патогенетическое значение в развитии неврологических нарушений при эпизодической печеночной энцефалопатии [1-3].
Высокий уровень азотистых продуктов приводит к избыточному образованию свободных радикалов, что способствует еще большему функциональному нарушению астроцитов. В то же время гипераммониемия вызывает образование дефектных нейромедиаторов и, как следствие, нарушение работы серотонинергической и глутаматергической систем, а также повышенную активность ГАМКергической системы. Гипоталамический центр насыщения — это одна из областей мозга, чувствительная к повышенному уровню аммиака. Результатом гипераммониемии у пациентов является отсутствие аппетита и, как следствие, возникновение белково-энергетического дефицита, который усугубляется катаболическими процессами, характерными для тяжелого цирроза печени. При циррозе печени повышается содержание серотонина в коре лобных долей. В норме серотонинергическая система участвует в регуляции циркадного ритма, двигательной активности, когнитивных и эмоциональных функций. Эти процессы нарушаются у пациентов с печеночной энцефалопатией. При печеночной энцефалопатии отмечаются изменения не только в серотонинергической системе, но и в глутаматергической регуляции, что способствует углублению когнитивных расстройств. Взаимосвязь между усилением гамкергических эффектов и развитием печеночной энцефалопатии возникает через активацию бензодиазепиновых рецепторов в головном мозге и связанное с этим увеличение синтеза нейростероидов. Помимо аммиака, марганец считается токсичным веществом, которое в последние годы оказывает неблагоприятное воздействие на структуры центральной нервной системы. Например, завышение его уровня вызывает гиперинтенсивность МР-сигнала в области бледного глобуса. Мнения экспертов об основном механизме патогенеза печеночной энцефалопатии расходятся. Некоторые исследователи считают, что гипераммониемия оказывает важное влияние на функцию нейронов. Другие придают основную роль изменениям аминокислотного состава и нарушениям нейромедиаторов (в частности, образованию ложных нейромедиаторов). Третьи обращают основное внимание на повышение концентрации меркаптана и уровня короткоцепочечных жирных кислот, что изменяет функцию ГАМК-бензодиазепинового комплекса. В последние годы активно формируется нейровоспалительная теория происхождения печеночной энцефалопатии, где важную роль играют глиальные элементы. Роль воспалительных изменений, вызванных персистенцией вируса, также обсуждается как возможная причина церебральных изменений при циррозе печени на фоне инфекции, вызванной вирусом гепатита С. Эти изменения приводят к нарушению метаболизма мозга. Результаты исследований по изучению мозгового кровотока и метаболизма при печеночной коме свидетельствуют о снижении их интенсивности, а также претерпевают обратное развитие при эффективном лечении с возобновлением нервно-психических функций.
Патогенетическая основа печеночной энцефалопатии с молниеносной печеночной недостаточностью несколько отличается от печеночной энцефалопатии с хроническим заболеванием печени. Молниеносная печеночная недостаточность развивается на фоне острого вирусного гепатита А, В, D, Е, при инфекции, вызванной вирусом простого герпеса, на фоне лекарственного поражения (при передозировке ацетаминофена), токсического поражения (при отравлении фосфором), как проявление болезни Вильсона-Коновалова, при острой жировой дистрофии или цитомегаловирусном гепатите у беременных женщин и других патологиях. Печеночная недостаточность классифицируется как молниеносная, если она развивается в течение 8 недель после первых симптомов заболевания или в течение 2 недель после клинического проявления желтухи. В картине молниеносной печеночной недостаточности на первый план выходят три клинических синдрома — гипокоагуляция, печеночная энцефалопатия, желтуха (последнее отмечается не всегда). Хроническая печеночная недостаточность отличается от печеночной энцефалопатии. При молниеносной недостаточности выражены отек головного мозга, внутричерепная гипертензия и грыжа. Фатальным фактором у 75-80% пациентов с печеночной энцефалопатией 4 стадии является отек головного мозга. Это объясняется следующими теориями. Согласно одному из них, глютамин, конечный продукт метаболизма аммиака, накапливается в астроцитах, что приводит к их набуханию. Другая теория предполагает ведущую роль нарушения церебральной ауторегуляции, приводящего к расширению сосудов, чрезмерному увеличению мозгового кровотока и отеку мозга. Конечно, оба этих механизма участвуют в развитии отека головного мозга при молниеносной печеночной недостаточности. Однако даже при благоприятном прогнозе относительно восстановления функции печени внутричерепная гипертензия вызывает снижение церебрального перфузионного давления и, как следствие, развитие ишемии, которая прогрессирует дальше после восстановления функции печени [1-3].
Т.к. печёночная энцефалопатия характеризуется гетерогенностью проявлений, в клинической картине доминируют [5]:
— когнитивные (варьирующие от минимальных изменений до комы) нарушения
— двигательные (ригидность мышц, затрудненная речь, тремор и др.) нарушения.
Печеночная энцефалопатия может прогрессировать медленно или быстро, а в некоторых случаях развивается стремительно, приводя к смерти в течение нескольких дней (молниеносное течение). В соответствии с критериями Уэст-Хейвена печеночная энцефалопатия классифицируется на основе уровня сознания, когнитивных функций и поведенческих расстройств, а также наличия или отсутствия неврологических и электрофизиологических изменений [1-3].
0 стадия — отсутствие клинически выраженных неврологических симптомов, расстройства выявляются только с помощью специальных нейропсихологических тестов [5].
I стадия — нарушения сна (сонливость днём и бессонница ночью), снижение внимания и концентрации. Эмоциональная нестабильность: депрессивное настроение, раздражительность, агрессия, тревога, плаксивость [5].
II стадия — нарастание интеллектуальных расстройств, проявляющихся на 1-й стадии. Углубление отмеченных психических расстройств с более выраженным неадекватным поведением (возможны бессмысленные поступки, эпизодическая агрессивность, бредовые состояния). Апатия, неряшливость, лёгкие эпизоды дезориентации во времени и пространстве. Речь пациента медленная и невнятная. Дизартрия, дисграфия (нарушение письма), астериксис [5].
III стадия — сонливость вплоть до ступора, значительная дезориентация во времени и пространстве, спутанность сознания при сохранении реакции на боль и (зрачков) на свет. Выраженные двигательные нарушения: тремор, существенные нарушения речи, повышенный тонус мышц [5].
IV стадия — наиболее тяжёлая, развитие комы. Нейропсихологические изменения: замедление психомоторных реакций и зрительно-пространственные нарушения [5]. Имеющиеся нейропсихологические нарушения приводят к затруднениям при вождении автомобиля.
Следует отметить, что у некоторых пациентов с печеночной недостаточностью в течение ряда лет наблюдаются только нарушения высших функций головного мозга (по результатам нейропсихологического тестирования) без каких-либо других неврологических симптомов [5].
При осмотре можно выявить [1, 2]:
-повышение мышечного тонуса
-замедленность движений
-атаксию
-постуральные расстройства или гиперрефлексию
-тремор (включая астериксис).
В некоторых случаях при печеночной энцефалопатии могут наблюдаться патологические непроизвольные движения [1-3]. Астериксис, или «трепещущий тремор», характерен для печеночной энцефалопатии и в конечном счете представляет собой миоклоническое нарушение осанки. Астериксис может быть как односторонним, так и двусторонним. В то же время это не является патогномоничным для печеночной энцефалопатии и может возникать при других состояниях — уремии, гиперкапнии, как осложнение при лечении карбамазепином или препаратами лития. Астериксис может возникать не только в руках, но и в других частях тела (ноги, полузакрытые веки).
Двусторонний астериксис более характерен для печеночной энцефалопатии и других дисметаболических расстройств, односторонний — для органического поражения головного мозга. В дополнение к неврологическим расстройствам, перечисленным выше, печеночная энцефалопатия проявляется нарушениями сна, пищевого поведения и сексуальной активности. Повреждение черепно-мозговых нервов не характерно (за исключением преддиагональных состояний, когда развивается тяжелый отек головного мозга), также выявляются нарушения чувствительности. Кроме того, может развиться полиневропатия. В таких случаях выпадают глубокие рефлексы или нарушается чувствительность полиневритического типа [1-3]. Результаты параклинических исследований имеют первостепенное значение. Отклонения в печеночных тестах (признаки цитолиза, печеночная недостаточность) указывают на возможное повреждение печени, но лабораторные изменения могут быть лишь слабо или умеренно выраженными [5]. Изменение уровня аммиака в артериальной крови, проведенное с соблюдением необходимых правил, несомненно, имеет значение для диагностики функции печени, однако было установлено, что оно слабо коррелирует с тяжестью неврологических расстройств. Интерпретация результатов исследования венозной крови неоднозначна, поскольку зависит от степени поступления аммиака из мышечной ткани, где он взаимодействует с аспартатом с образованием глютамина. Однако при тяжелой печеночной энцефалопатии уровень аммиака в крови может быть нормальным или слегка повышенным. Для диагностики минимальной печеночной энцефалопатии используют нейропсихологические и нейрофизиологические (ЭЭГ, вызванные потенциалы) методы, иногда дополняя их методами [5]. Методы структурной нейровизуализации в основном используют для исключения структурных повреждений головного мозга у больных циррозом печени, у которых отмечается повышение интенсивности сигнала в области бледного шара при проведении МРТ в Т1-режиме. Повышение интенсивности сигнала при МРТ в Т1-режиме визуализируется не только в области бледного шара: схожие изменения описаны в других областях головного мозга, включая пирамидную и экстрапирамидную системы, лимбическую область. Увеличение концентрации марганца также играет роль в механизме развития печеночной энцефалопатии, поэтому предположения о связи увеличения интенсивности сигнала во время МРТ в режиме Т1 с накоплением этого элемента в этих областях мозга вполне понятны. Протонная МР-спектроскопия используется для оценки роли нарушений церебрального метаболизма в печеночной энцефалопатии. С помощью этой методики выявляется относительно стабильная картина изменений в виде увеличения глутамат-глютаминового комплекса, снижения содержания холина и миоинозитола, а также присутствия N-ацетиласпартата. Используя магнитное поле очень высокой мощности, можно дифференцировать сигналы глютамина и глутамата. Подобные изменения обнаруживаются даже при эпизодической печеночной энцефалопатии. Несмотря на довольно высокую специфичность этих данных, МР-спектроскопия не превосходит по чувствительности другие методы, особенно нейропсихологические [5]. Подчеркивается необходимость дальнейших исследований в этом направлении для лучшего понимания патогенеза печеночной энцефалопатии. Печеночная энцефалопатия, как следствие молниеносной печеночной недостаточности, характеризуется некоторыми особенностями клинических проявлений. У значительной части пациентов развитию печеночной энцефалопатии предшествует желтуха [1-3]. Печеночная недостаточность быстро нарастает с исходом в кому. На начальной стадии отмечаются тошнота, рвота, боли в животе в сочетании с нервно-психическими расстройствами, такими как бред или мания. На 2-й и 3-й стадиях печеночной энцефалопатии — астериксис. Переходу к 3-й и 4-й стадиям печеночной энцефалопатии обычно предшествует возбуждение пациентов и галлюцинации. В некоторых случаях течение печеночной энцефалопатии настолько злокачественное и молниеносное (из-за массивного некроза печени), что у пациентов не успевает развиться желтуха [1-3]. В этих случаях увеличение протромбинового времени имеет особое значение в диагностике.
References
1. Новицкий, В.В. Патофизиология: учебник: в 2 т. //Под ред. В.В. Новицкого, О.И. Уразовой. /5-е изд., перераб. и доп.– М.: ГЭОТАР-Медиа.– 2018.– Т.1.– С. 896.2. Литвицкий П.Ф. Патофизиология. //Под ред. П.Ф. Литвицкий учебник /7-е изд., перераб. и доп.- ГЭОТАР-Медиа. – 2021. – С.864.
3. Черешнев В.А. Клиническая патофизиология: курс лекций //Под ред. В.А. Черешнева, П.Ф. Литвицкого, В.Н. Цыгана. – СПб.: СпецЛит.– 2015.– С. 432.
4. Смолина С.П., Петрова М.М., Шаробаро В.И., Якубов Д.А. Особенности патогенеза и клинического течения печёночной энцефалопатии при алкогольном циррозе печени // ВНМТ. – 2013. – №1. – С. 84-88.
5. Вьючнова Е.С., Бабина С.М. Дифференциальная диагностика и лечение печёночной энцефалопатии // Consilium Medicum. ¬¬¬¬– 2017. – №8. – С. 84-88.
